Anvisa aprova primeiro medicamento injetável para prevenir infecção do vírus HIV
Ainda não há uma data para o início da comercialização e também não há informações se ele será oferecido pelo SUS
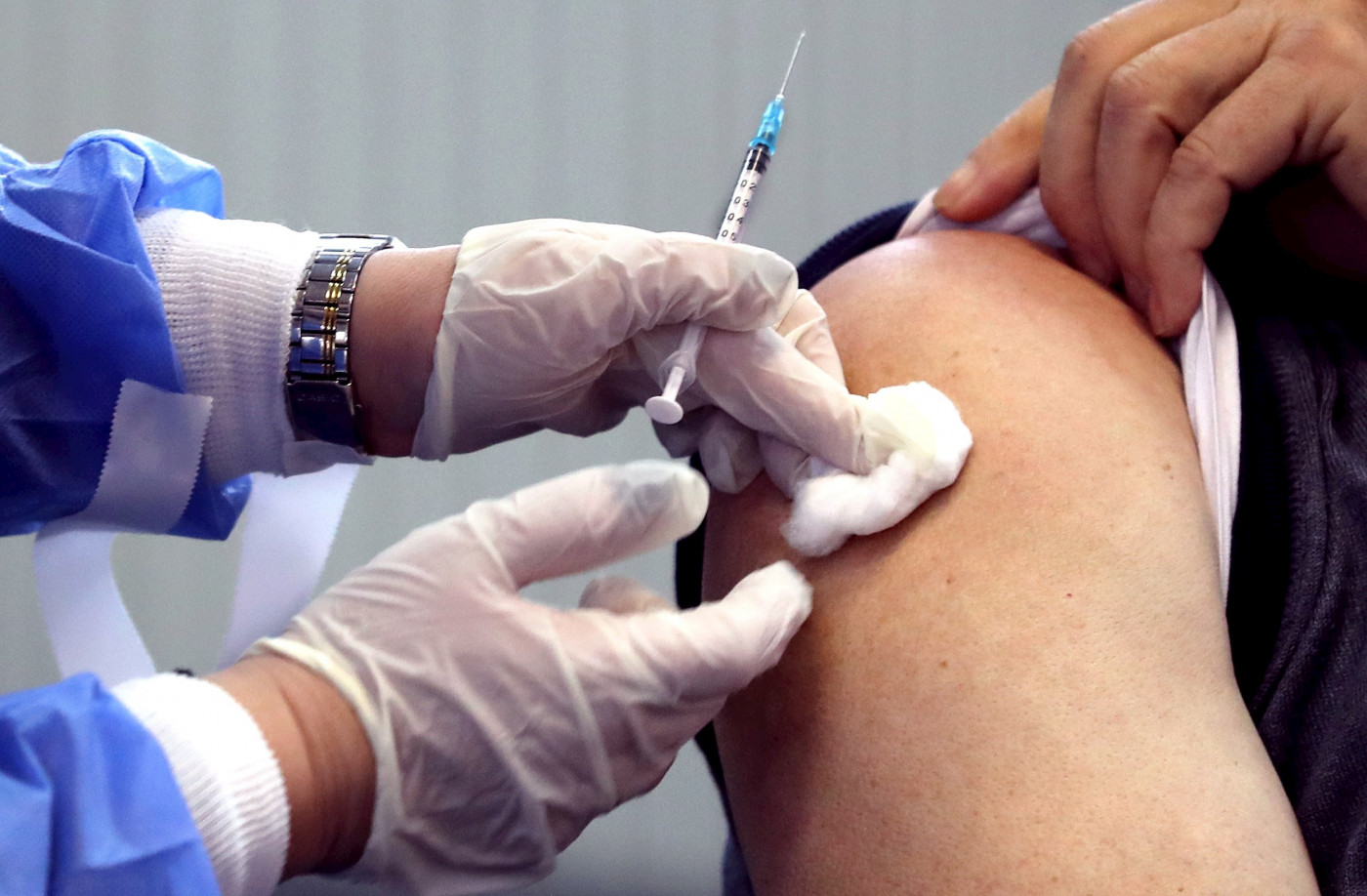
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o cabotegravir, o primeiro medicamento injetável contra o HIV no Brasil. A autorização para o uso do medicamento foi dada à farmacêutica britânica GSK e publicada no Diário Oficial da União (DOU) no dia 5 de junho, contudo, ainda não há uma data para o início da comercialização no Brasil e também não há informações se ele será oferecido pelo SUS (Sistema Único de Saúde) de forma imediata. A PrEP injetável é considerada a mais recente inovação para prevenção do HIV. Ele atua como uma profilaxia pré-exposição ao vírus causador da aids e diferente dos outros medicamentos para prevenir a infecção pelo vírus, ele tem uma ação prolongada. O cabotegravir também é conhecido como apredute – nome comercial -, e recebeu autorização da FDA (Food and Drug Administration), agência reguladora de saúde dos Estados Unidos, em 2021. No ano passado, o medicamento chegou a ser recomendado pela OMS (Organização Mundial da Saúde) como parte de uma abordagem abrangente para a prevenção do HIV. O cabotegravir é uma injeção aplicada a cada dois meses para prevenir a infecção pelo HIV. A injeção foi desenvolvida pela farmacêutica GSK. Atualmente, no Brasil, está em curso uma estratégia oferecida pelo SUS por meio de comprimidos diários. A terapia é destinada a determinados grupos considerados de maior risco de exposição ao HIV, como homens que fazem sexo com outros homens, profissionais do sexo e pessoas que não vivem com o vírus, mas estão em um relacionamento sorodiscordante. A principal diferença entre os remédios que já estão em curso e esse novo são: sua ação prolongada e o fato do remédio ser injetável. Com isso, há uma melhor adesão do tratamento.



Comentários
Conteúdo para assinantes. Assine JP Premium.