Fiocruz deve submeter dados para aprovação de vacina de Oxford no Brasil até 15 de janeiro
Informação foi confirmada pela fundação na tarde desta quarta-feira, pouco após reunião entre farmacêutica AstraZeneca e Agência Nacional de Vigilância Sanitária
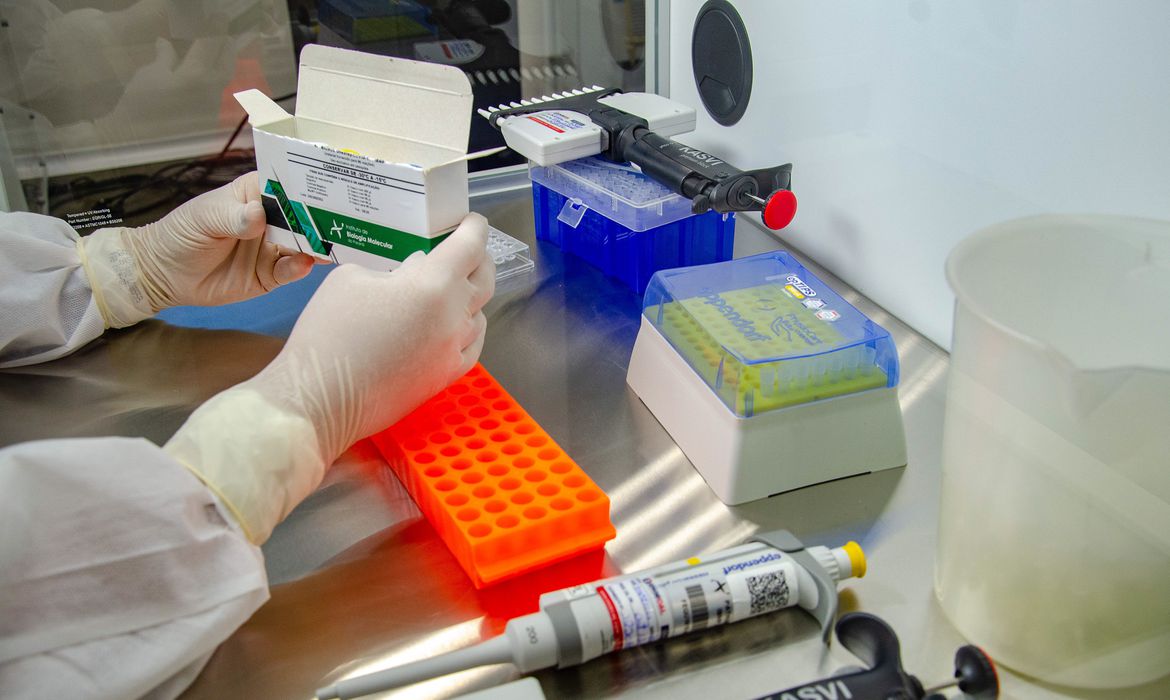
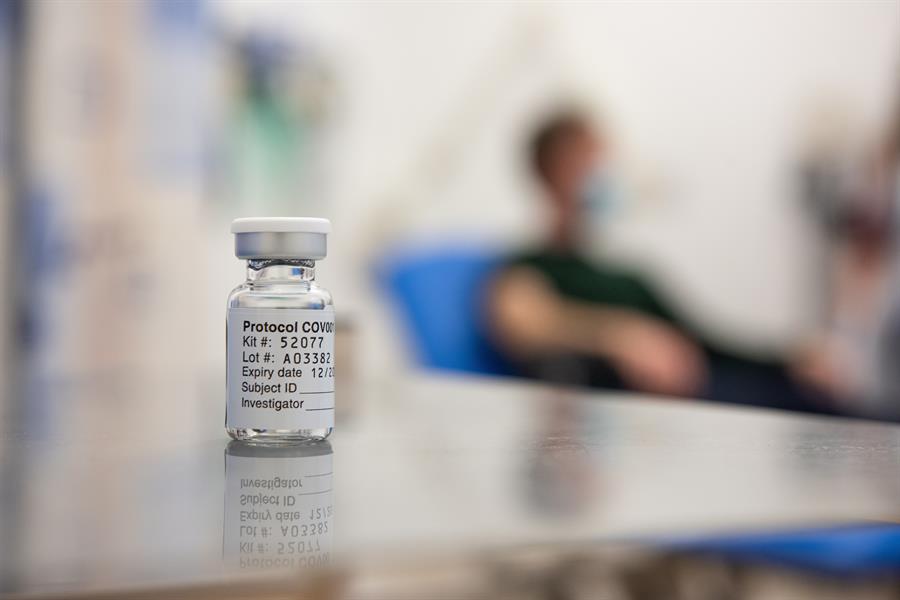
A Fundação Oswaldo Cruz (Fiocruz) deve pedir até o dia 15 de janeiro a aprovação da Agência Nacional de Vigilância Sanitária (Anvisa) para uso da vacina de Oxford contra a Covid-19 de forma emergencial no Brasil. A informação foi dada poucas horas após uma reunião entre a agência reguladora brasileira e representantes do laboratório AstraZeneca, que tem parceria com a fundação no país para realizar testes da vacina em voluntários. Em nota divulgada nesta quarta-feira, 30, a Fiocruz celebrou a aprovação do uso do imunizante no Reino Unido e disse que esse processo pode ajudar a acelerar a aprovação em terras brasileiras. O órgão afirmou, ainda, que tem como proposta entregar 100,4 milhões de doses até o final do primeiro semestre de 2021. No segundo semestre, 110 milhões de doses devem ser fabricadas e entregues.
A partir do momento que a documentação com o pedido de uso emergencial da vacina no Brasil for formalizada, a Anvisa terá prazo de até dez dias corridos para aprovar o uso. Pelo menos oito mil voluntários brasileiros receberam doses da vacina durante a fase de testes no país. Em entrevista ao “Jornal Jovem Pan” na tarde desta quarta-feira, a professora da Universidade Federal de São Paulo (Unifesp), afirmou que nenhum dos voluntários que recebeu a vacina desenvolvida por Oxford apresentou forma grave da doença ou foi hospitalizado por causa da Covid-19. A previsão da Fiocruz é que as primeiras doses da vacina sejam entregues ao Ministério da Saúde no dia 8 de fevereiro. Um dos pontos ressaltados pela fundação em relação à vacina de Oxford é que elas são conservadas em temperaturas entre 2ºC e 8ºC, o que permite que ela seja transportada com maior facilidade.


Comentários
Conteúdo para assinantes. Assine JP Premium.