Taxa de eficácia global da CoronaVac é de 50,38%, diz Instituto Butantan
Até o momento, não foi registrado nenhum evento adverso grave relacionado à vacinação; reações alérgicas ocorreram em 0,3% dos participantes

O Instituto Butantan divulgou nesta terça-feira, 12, os dados completos sobre a eficácia da CoronaVac contra a Covid-19. Segundo revelado nesta terça, a vacina atingiu eficácia global de 50,38% – a Anvisa exige, no mínimo, 50%. Anteriormente, o governador de São Paulo, na última quinta-feira, 7, João Doria havia revelado os recortes de eficácia da vacina, que é 78% eficaz para casos leves da Covid-19 e 100% eficaz na prevenção de casos graves e moderados da doença. Apesar disso, pesquisadores e especialistas cobravam a divulgação da taxa de eficácia geral do imunizante, que consiste na comparação de quantas pessoas ficaram doentes entre os grupos de vacinados e daqueles que apenas receberam o placebo, sem recorte de grupo, ou seja, a capacidade da vacina proteger em todos os casos.
“Nós utilizamos a definição de caso mais abrangente possível. Outros estudos de outros fabricantes, não incluiriam como possível caso uma pessoa com dois dias de dor de cabeça, mesmo que tivesse um teste positivo de PCR, nós incluímos. Ou dois dias de coriza, nós incluímos. A gente abaixou bastante a barra para poder realmente detectar até o caso mais leve possível e isso faz uma diferença que prejudica a comparabilidade desse estudos com outros estudos”, explicou Ricardo Palácios, diretor médico de pesquisa clínica do Instituto. Palácios afirmou que a taxa de eficácia menor é consequência da escolha “consciente” do Instituto para que a pesquisa atingisse mais rápido o número mínimo de casos positivos necessários para a fase 3. “A gente estava sacrificando eficácia para aumentar o número de casos e ter uma resposta mais rápida. Essa foi uma decisão pensada, arriscada, mas a gente precisava dessa resposta rápido”, completou o diretor de pesquisa.
Segundo Alex Precioso, diretor do Centro de Segurança Clínica e Gestão de Risco Farmacoepidemiológica do Butantan, até o momento, não foi registrado nenhum evento adverso grave relacionado à vacinação. Reações alérgicas ocorreram em 0,3% dos participantes, não foi observada reação anafilática e sem diferenças entre grupo experimental e placebo. Foram 4.653 vacinados com a CoronaVac e 4.599 receberam o placebo. Nenhum participante do grupo vacinal e sete participantes do grupo placebo apresentaram a forma grave da doença ou precisaram de internação, resultando na eficácia de 100%. “Este um dado ainda pequeno, não tem significância estatística, embora demonstre uma tendência que precisaremos de mais tempo e estudo para acompanhar se ela se confirma”, disse Ricardo Palácios.
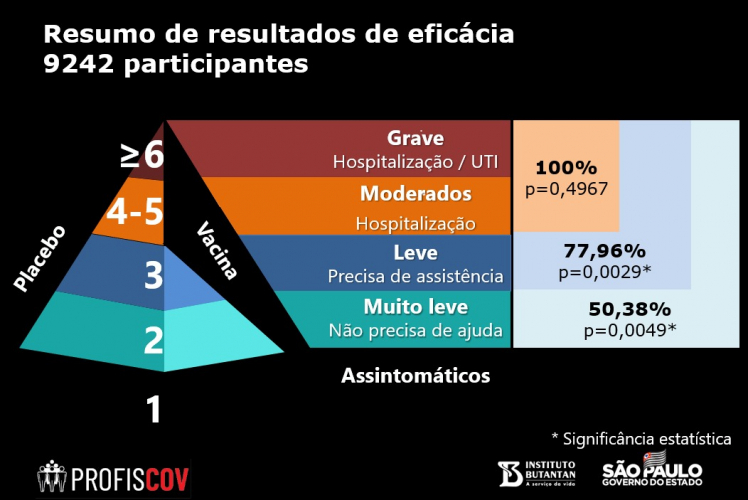
Reprodução/Instituto Butantan
Entre os casos que precisam de alguma assistência, seja ela ambulatorial ou hospitalar, foram registrado 38 casos dentro do estudo, sendo que 7 receberam o imunizante e 31, o placebo, determinando a eficácia de 77,96%. O estudo registrou 252 casos positivos de Covid-19, sendo que 85 receberam a vacina e 167, o placebo. Segundo o Instituto, a eficácia vacinal para diminuir a Covid-19 foi demonstrada em situação de alta exposição e o efeito tende a aumentar conforme aumenta a intensidade da doença. O estudo ainda não pode terminar o efeito da CoronaVac sobre a transmissão.
Trajetória da CoronaVac
O diretor Dimas Covas relembra que em abril de 2020 a vacina já estava pronta na China. O modelo de imunizante utilizado pela Sinovac já estava desenvolvido para o primeiro coronavírus, o Sars-CoV-1. A empresa, então, aproveitou a tecnologia para a nova forma do vírus, agilizando o processo e fazendo com que a CoronaVac fosse uma das primeiras vacinas a ficarem prontas. Os testes pré-clínicos, realizados em animais, foram iniciados já em abril. Os estudos seguiram para a fase 1 e fase 2 na China até que o Instituto Butantan foi encarregado de realizar a fase 3 da vacina.
Os profissionais da saúde foram escolhidos como voluntários por estarem em ambientes com alta carga viral circulando, com incidência de 20% do coronavírus. “É a população que desafia a vacina de forma mais intensa, é o teste mais duro que uma vacina pode enfrentar”, argumentou Dimas Covas. Além de um estudo que está em andamento, o Instituto Butantan realizará mais quatro estudos sobre o imunizante. Por parte da Sinovac, a vacina está sendo testada na Turquia, na Indonésia e no Chile. “É uma vacina que está esperando para ser usada”, disse.
Na quinta-feira, 7, quando os dados preliminares foram divulgados, o Butantan e a Anvisa tiveram uma reunião de pré-submissão do imunizante na qual a instituição apresentou os dados consolidados à agência. No dia seguinte, o instituto enviou o pedido oficial para o uso emergencial da vacina à Agência Nacional de Vigilância Sanitária (Anvisa). No entanto, no dia seguinte, o órgão regulador cobrou a submissão de mais informações sobre a vacina. Desde a oficialização do pedido, a agência reguladora possui o prazo de dez dias para conceder ou não o registro de emergência da CoronaVac.



Comentários
Conteúdo para assinantes. Assine JP Premium.