Covid-19: Conheça as 6 vacinas mais avançadas contra a doença
Das 6 imunizações que estão em estágio mais avançado, 3 estão sendo testadas no Brasil e uma deve começar em breve; governo do Estado de São Paulo prevê que a vacina chinesa Sinovac pode estar disponível em janeiro de 2021
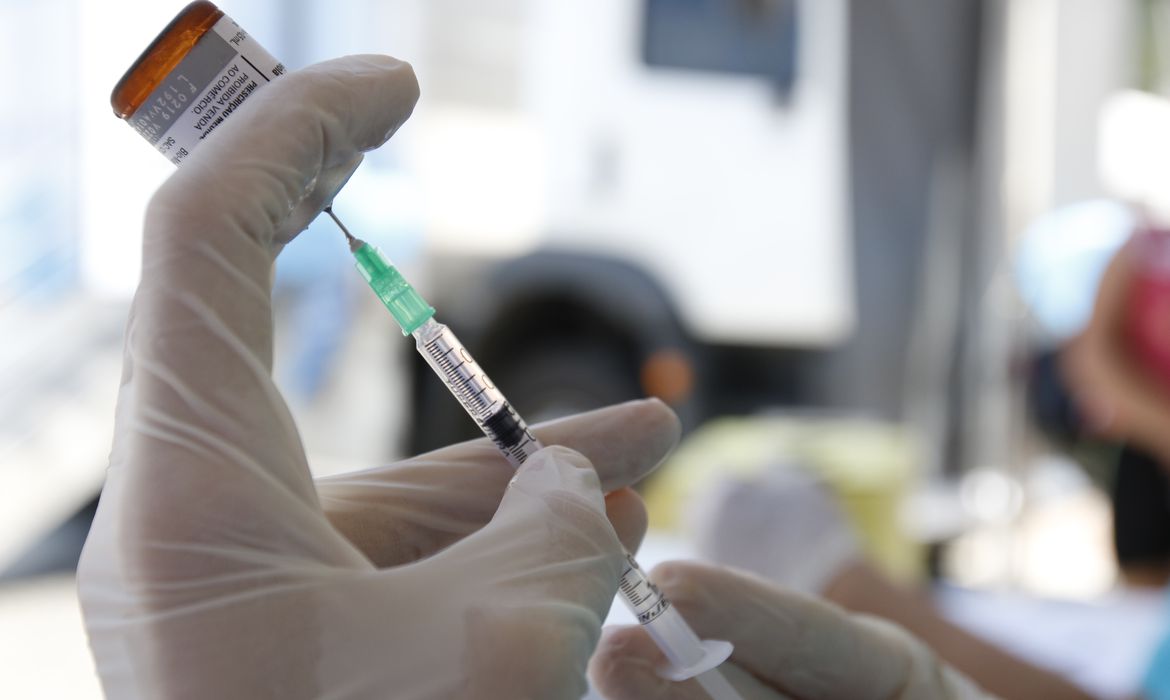
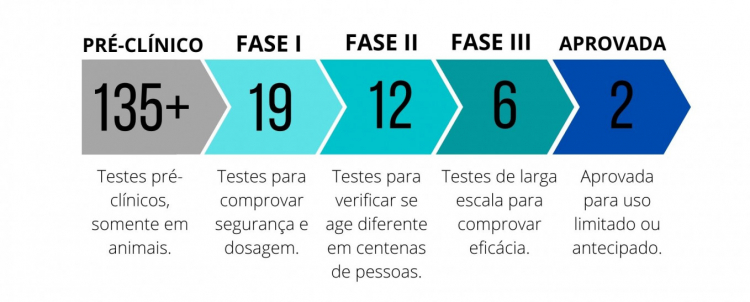
O desenvolvimento de uma vacina normalmente leva anos de pesquisas e testes até estar disponível para a aplicação em humanos. No entanto, a corrida pela vacina contra a Covid-19 está mobilizando cientistas em todo o mundo, ao ponto de alguns mais otimistas falarem em uma imunização em larga escala já para o início de 2021. Atualmente, são mais de 160 vacinas em estudo, cerca de 140 na fase pré-clínicas — quando ainda não foram testadas em humanos –, 19 na fase 1, 12 na fase 2, seis na fase 3, e duas já aprovadas para uso limitado. Uma delas é a chinesa CanSino, liberada para uso militar; e a outra é a vacina russa, anunciada pelo presidente Vladimir Putin no dia 11 de agosto. O infectologista da BP, Beneficência Portuguesa de São Paulo, Heber Azevedo, afirma que alguns fabricantes dizem que “é possível que exista uma vacina para casos emergenciais a partir de outubro deste ano”. No entanto, ele ressalta que isso é “uma expectativa, pois nada garante que os resultados da fase 3 serão satisfatórios”.
As primeiras pesquisas começaram ainda em janeiro, quando as contaminações pelo novo coronavírus explodiram na China. Nesta época, cientistas decifraram o genoma do SARS-Cov-2. Já os primeiros testes em humanos foram feitos em março, com resultados pouco conclusivos. Atualmente, três vacinas na fase 3 estão sendo testadas no Brasil, e uma vai começar os testes em breve. No dia 18 de agosto, a Anvisa aprovou a condução do ensaio clínico da vacina Ad26.COV2.S, desenvolvida pela Janssen Pharmaceuticals, do grupo Johnson & Johnson. Dos 60 mil voluntários que vão receber uma dose da vacina ou de placebo, 7 mil deles serão brasileiros. Os estados que vão participar são: São Paulo, Rio Grande do Sul, Rio de Janeiro, Paraná, Minas Gerais, Bahia e Rio Grande do Norte. Trata-se de um estudo na fase 3, randomizado, duplo cego e controlado por placebo. De acordo com a Anvisa, essa potencial vacina é composta de um vetor recombinante, não replicante, de adenovírus tipo 26 (Ad26), construído para codificar a proteína S (Spike) do vírus SARS-CoV2.
Vacinas aprovadas para uso limitado:
1) Vacina da CanSino
A empresa chinesa CanSino Biologics desenvolveu uma vacina baseada em um adenovírus chamado Ad5, em parceria com o Instituto de Biologia da Academia de Ciências Médicas Militares do país. Em maio, eles publicaram resultados promissores de um teste de segurança da fase 1 e, em julho, relataram que seus testes da fase 2 demonstraram que a vacina produziu uma forte resposta imunológica. Em 25 de junho, os militares do país aprovaram a vacina por um ano por ser uma “droga especialmente necessária”. Em 9 de agosto, o ministério da saúde da Arábia Saudita anunciou que a empresa realizaria um teste de fase 3 no país. No dia 17 de agosto, o Escritório de Propriedade Intelectual da China, Sipo, na sigla em inglês, aprovou a primeira patente para a vacina da CanSino.
2) Vacina Russa
No dia 11 de agosto, o presidente da Rússia, Vladimir Putin, anunciou a primeira vacina registrada contra a Covid-19 e, no dia 17, o diretor do Instituto Gamaleya de Microbiologia e Epidemiologia, que desenvolveu o imunizante Sputnik V, disse que a vacinação em massa começará dentro de um mês no país. Há muita desconfiança entre a comunidade científica, no entanto, a respeito da confiabilidade do composto, já que a Rússia não divulga informações sobre as pesquisas ou método de elaboração da fórmula.
O estado do Paraná começou as tratativas para possível acordo e obtenção da vacina russa. Em entrevista à Jovem Pan, o diretor-presidente do Tecpar (Instituto de Tecnologia do Paraná), Jorge Callado, afirmou que a importação do imunizante, assim como o compartilhamento da tecnologia para fabricação, depende do resultados de testes clínicos e da autorização dos órgãos reguladores. Segundo ele, o Paraná será o “braço técnico executor do acordo para a realização dos testes da Fase 3” da vacina, “uma vez que as etapas 1 e 2 já foram realizadas na Rússia”. Com isso, o governo estadual solicitará autorização da Anvisa para realização dos testes clínicos no estado e, “com resultados promissores será confirmada a segurança, eficácia e eficiência” da vacina. Mesmo com as opiniões contrárias, a expectativa do governo do Paraná é que doses possam ser importadas ainda neste ano, caso “a fase de testes seja muito positiva e se obtenha o registro no Brasil”, explica Jorge Callado.
Vacinas que estão na fase 3 de testes:
Segundo um balanço atualizado em 10 de agosto pela Organização Mundial da Saúde (OMS), apenas seis vacinas estão na fase 3 de estudos. É somente depois desta prova, em milhares de participantes, que ela pode ou não ser licenciada e liberada para a comercialização. As pessoas também precisam ser acompanhadas por meses, para demonstrar que há poucas infecções entre as que receberem a vacina na comparação com aquelas que receberam um placebo. Só assim as imunizações poderão ser aprovadas por órgãos reguladores — como a Anvisa aqui no Brasil.
1) Vacina de Oxford
Da farmacêutica AstraZeneca, a vacina integra a parceria da Universidade de Oxford (Reino Unido) com a Unifesp (Universidade Federal de São Paulo). Ela está na fase 3 de testagem, aplicada em voluntários no Reino Unido, África do Sul e Brasil, sendo 5 mil voluntários em São Paulo, Rio de Janeiro e Salvador. Em 20 de julho, cientistas de Oxford afirmaram que a vacina é segura e induz resposta imunológica. As informações foram divulgadas pela revista médica “The Lancet”. A dose levou os voluntários a produzir anticorpos e glóbulos brancos que podem combater o coronavírus, mas ainda é cedo para saber se isso é suficiente. A estimativa é que doses emergenciais possam ser entregues ainda em outubro, e que a disponibilização em larga escala aconteça em abril de 2021. O CEO da companhia farmacêutica AstraZeneca, Pascal Soriot, deu perspectivas ainda mais otimistas. Segundo ele, se os resultados dos testes forem bem-sucedidos, a população do Reino Unido pode ter acesso à vacina ainda em setembro deste ano. Essa imunização é considerada a mais promissora pela comunidade científica mundial. Isso porque o antiviral já tinha sido estudado para a Síndrome Respiratória Aguda Grade (Sars) e a Síndrome Respiratória do Oriente Médio (Mers), também causadas pelo coronavírus. Assim, o processo e a segurança tiveram etapas aceleradas.
2) Vacina da Moderna
O laboratório Moderna afirmou no final de julho que iniciou o estágio final de testes em uma candidata a vacina para a Covid-19, com apoio do governo dos Estados Unidos. Esta é a primeira pesquisa a ser implementada no programa anticoronavírus Operation Warp Speed, do governo de Donald Trump. As notícias do estudo, que testará a resposta à vacina em 30 mil adultos sem registro da doença respiratória, aumentaram as ações da Moderna na Bolsa de Valores em 11%. Em comunicado, a Moderna afirmou que poderá fabricar entre 500 milhões e 1 bilhão de doses por ano a partir de 2021, após chegar a um acordo de colaboração com a empresa suíça Lonza, que garantiu a distribuição das doses necessárias para a conclusão do estudo.
3) Pfizer e Biontech
A vacina desenvolvida por pesquisadores de laboratórios dos Estados Unidos e da Alemanha das empresas Pfizer e Biontech está na fase 3 de testes, e conseguiu aprovação em via rápida pelo órgão regulador dos Estados Unidos, a FDA. No dia 5 de agosto, a imunização começou a ser testada em voluntários brasileiros, que têm entre 18 e 85 anos. No dia 22 de julho, a Anvisa aprovou a testagem da vacina em mil voluntários das cidades de São Paulo e Salvador, que podem ser de quaisquer áreas de atuação, desde que expostos ao vírus. A Pfizer já concordou em vender 100 milhões de doses de sua vacina ao governo dos Estados Unidos, oferecendo uma opção de compra de mais 500 milhões. Um artigo publicado no dia 20 de julho como prévia (pré-print) apontou que a substância é segura e capaz de induzir resposta imunológica. De acordo com as farmacêuticas, foram verificadas respostas imunes “fortes”, e em velocidade anterior ao prazo estimado, das chamadas células T, consideradas fundamentais para protegerem um organismo do novo coronavírus.
4) CoronaVac
O governador de São Paulo, João Doria, anunciou no dia 27 de julho que a vacina chinesa Sinovac Biotech, produzida em parceria com o Instituto Butantan, pode estar disponível em janeiro de 2021 no Sistema Único de Saúde (SUS). “Abril do ano que vem já teremos, com toda segurança, a imunização e a tranquilidade que as pessoas poderão celebrar festas, atividades, eventos musicais ou esportivos, sem risco para sua saúde ou sua vida”, afirmou o governador. A vacina está na fase 3, sendo administrada em mais de 9 mil voluntários no país. O Butantan recebeu 20 mil doses do imunizante e de placebo que serão distribuídas para 12 centros de referência. A conclusão dessa etapa deve ocorrer em outubro. A Sinovac está construindo uma fábrica de vacinas, que deverá ficar pronta neste ano e pode ser capaz de produzir até 100 milhões de doses anualmente. Em junho, a companhia anunciou que as fases 1 e 2 em 743 voluntários produziram uma resposta imune e não trouxeram efeitos adversos graves.
5) Vacina da Sinopharm
Depois de descobrir que uma vacina inativada contra o vírus era segura e provocou uma resposta imune, a empresa estatal chinesa Sinopharm começou a fazer, em julho, testes da fase 3 nos Emirados Árabes. O ministro da Saúde de Abu Dhabi foi o primeiro voluntário a ser imunizado e 15 mil pessoas devem participar no total. Em julho, o presidente da Sinopharm disse que a vacina poderia estar disponível para a população até o fim deste ano. A Sinopharm também está testando uma segunda vacina de vírus inativado, desenvolvida pelo Instituto de Produtos Biológicos de Pequim. Os testes estão na fase 3, também nos Emirados Árabes Unidos, onde 5 mil pessoas recebem a versão do Instituto Wuhan, enquanto outras 5 mil a do Instituto de Pequim.
6) Vacina contra a tuberculose
Estudos estão sendo conduzidos na Holanda (Nijmegen’s Radboud University and Utrecht University), Grécia (University of Athens), Austrália (University of Melbourne) e Reino Unido (University of Exeter) para avaliar se a vacinação contra o bacilo Calmette-Guérin (BCG) poderia aumentar resistência a infecções em geral, como à Covid-19, em profissionais de saúde e idosos. Na Austrália, os testes estão na fase 3. Um estudo conduzido pela Universidade de Michigan, nos Estados Unidos na revista Science Advances, indicou que os países onde a vacina contra as formas graves da tuberculose é obrigatória apresentaram taxas mais baixas de infecção e morte pelo coronavírus durante o primeiro mês da pandemia em suas regiões.

Entenda as fases da pesquisa
O processo de pesquisa e desenvolvimento de uma nova vacina é constituído de diversas etapas. A primeira corresponde à pesquisa básica e é onde novas propostas de imunização são identificadas. Já a segunda, é a realização dos testes pré-clínicos, para demonstrar a segurança e o potencial imunogênico da vacina. A terceira etapa são os ensaios clínicos, que é a mais longa e a mais cara do processo, em que são feitos os estudos de fase 1, fase 2, fase 3 e fase 4.
O infectologista da Beneficência Portuguesa de São Paulo explica que, após a fase 3, há outros pontos a serem avaliados: em quais faixas etárias e populações — cardiopatas, pneumopatas, obesos, grávidas, a vacina produziu anticorpos; qual o nível destes anticorpos no sangue; por quanto tempo eles se mantém em nível protetor e se foram capazes de proteger a pessoa. Além disso, será avaliado também a segurança da vacina, os efeitos colaterais, a frequência e a intensidade com que acontecem e as complicações que poderão causar. “A disponibilidade de uso para a população geral dependerá da capacidade do fabricante de produzir a vacina e da competência dos governos em distribuí-las. É possível, e espero que aconteça, ter no futuro duas ou mais vacinas disponíveis ao mesmo tempo”, diz Azevedo.
- Ensaio pré-clínico: A vacina é administrada em animais como camundongos ou macacos para verificar se ela produz uma resposta imune.
- Fase 1: Cientistas administram a vacina em um pequeno número de pessoas para testar a segurança e a dosagem, além de confirmar que ela estimula o sistema imunológico.
- Fase 2: Cientistas administram a vacina a centenas de pessoas divididas em grupos, como crianças e idosos, para verificar se age de maneira diferente.
- Fase 3: Os cientistas dão a vacina a milhares de pessoas e esperam para ver quantos são infectados, em comparação com os voluntários que receberam placebo.


Comentários
Conteúdo para assinantes. Assine JP Premium.