Vacina contra a Covid-19: Quando começa? Todos brasileiros serão vacinados? Quantas doses o Brasil já tem?
Para especialistas, os imunizantes também serão eficazes na proteção contra a nova variante do coronavírus, encontrada no Reino Unido e também no Rio de Janeiro

As discussões sobre a vacinação contra a Covid-19 no Brasil chegaram ao Supremo Tribunal Federal (STF), criaram um embate entre governadores e o presidente Jair Bolsonaro, e trouxeram grande expectativa na população em 2020. Em meio a um aumento de casos e mortes no País, o que fez com que várias regiões voltassem atrás na flexibilização das medidas restritivas contra o coronavírus, os brasileiros querem saber quando vai, de fato, começar a imunização e como ela será feita. Para especialistas, provavelmente teremos mais de uma vacina aprovada e sendo usada no País. Até agora, as farmacêuticas responsáveis pelos imunizantes da Aztrazeneca, desenvolvida em parceria com a Fiocruz, e dos laboratórios Pfizer e BioNTech, entregaram resultados de fase 3 para a Agência Nacional de Vigilância Sanitária (Anvisa). No dia 23, o Instituto Butantan, de São Paulo, que produz a vacina em parceria com a Sinovac, adiou a apresentação dos resultados, pois a farmacêutica chinesa pediu que o parceiro brasileiro encaminhasse os dados para que eles sejam computados e apresentados de forma conjunta com testes realizados em outros países. Porém, o instituo afirma os testes da fase 3 alcançaram o nível exigido. A vacina da Janssen, da Johnson&Johnson, também realiza testes no País, porém ainda não entregou a documentação. “O que a gente espera é que o máximo de vacinas possam chegar ao Brasil. Com apenas um fabricante é muito pouco provável que a gente consiga vacinar muitas pessoas, que é o que mundo inteiro deseja. Começamos pelos grupos de maior risco, mas para que a gente possa se livrar da Covid-19, precisamos de um número maior de pessoas vacinadas”, diz a vice-presidente da Sociedade Brasileira de Imunizações (SBIm), Isabella Ballalai.
Já o infectologista da BP – A Beneficência Portuguesa de São Paulo, João Prats afirma que, se implementada rápido, a vacinação provavelmente vai evitar um aumento grande no número de casos. “Não é que nem o isolamento, que você só diminui o contato entre as pessoas suscetíveis. Não é que vai achatar a curva, a curva vai cair mesmo”, ressaltou. O ministro da Saúde, Eduardo Pazuello, disse no último dia 22 que espera ter 15 milhões de doses da vacina de Oxford, produzida pela Fundação Oswaldo Cruz (Fiocruz), disponíveis até o fim de janeiro. No dia 13 de dezembro, uma nova variante do coronavírus foi identificada no Reino Unido e, em 22 de dezembro, pesquisadores do Laboratório Nacional de Computação Científica (LNCC) e da Universidade Federal do Rio de Janeiro (UFRJ) encontraram uma nova mutação no Rio de Janeiro, que surgiu em julho e foi detectada pela primeira vez em outubro. A principal preocupação da população mundial é qual o impacto que a nova variante terá na produção de vacinas contra a Covid-19. A Organização Mundial da Saúde (OMS), no entanto, já se manifestou afirmando que não existem evidências de que a variação cause uma infecção mais grave ou afete a eficácia dos imunizantes já desenvolvidos. “A mutação não é motivo de preocupação para a vacina, é motivo de preocupação a curto prazo por conta da transmissão da doença”, diz o doutor em virologia e professor adjunto da Faculdade de Medicina de São José do Rio Preto, Maurício Lacerda Nogueira. “O aparecimento de novas cepas é um fenômeno natural com pouquíssimo impacto, se é que tem algum, nas vacinas. São mutações muito pontuais que não afetam a resposta dos nossos imunizantes. Então, isso não é motivo de preocupação para a vacina”, continua. O professor ressalta que, apesar de cada vacina ter uma tecnologia diferente e ter suas vantagens e desvantagens, esse tipo de mutação pontual e considerada natural não afeta nenhum dos imunizantes desenvolvidos em um primeiro momento.
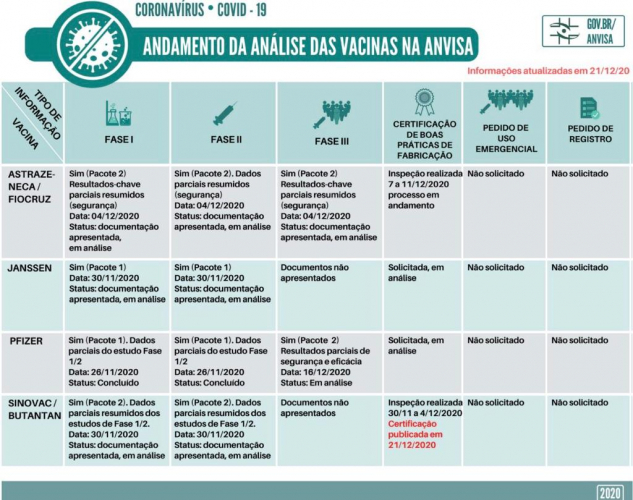
Reprodução/Anvisa
Quando começará a vacinação no Brasil?
Em audiência pública na Comissão Externa de Enfrentamento à Covid-19, da Câmara dos Deputados, no último dia 22, o ministro da Saúde, Eduardo Pazuello, disse que a “melhor hipótese” para o início da vacinação contra o coronavírus será no final de janeiro, e a pior, entre o meio e o final de fevereiro. Até agora, o líder da pasta já previu o começo da imunização para várias datas, como março de 2021 e dezembro de 2020. Pazuello indicou, também, que os estados não terão autonomia. Em São Paulo, o governador João Doria (PSDB) afirma que a vacinação terá início em 25 janeiro. A estratégia planejada pelo governo inclui a CoronaVac, produzida pelo Instituto Butantan em parceria com a Sinovac. Pazuello afirmou, em documento enviado ao Supremo Tribunal Federal (STF), que a primeira etapa da imunização contra o novo coronavírus deve iniciar cinco dias após a aprovação de uma das vacinas pela Anvisa. Ele evitou, porém, definir uma data, já que até o momento não há um imunizante aprovado no Brasil. Foram apresentados e estão em análise resultados parciais de Fase 3 das vacinas da Universidade de Oxford e da Pfizer. Porém, nenhum dos laboratórios solicitou, ainda, o uso emergencial ou o pedido de registro, essenciais para a comercialização dos imunizantes no País. No dia 14 de dezembro, a Anvisa fixou um prazo máximo de dez dias para decidir sobre a autorização emergencial do uso de vacinas contra a Covid-19. No entanto, para o cumprimento desse prazo, é necessário que as empresas solicitantes tenham apresentado todos os documentos necessários à análise. O Instituto Butantan, que desenvolve a vacina CoronaVac junto com o laboratório chinês, afirmou que solicitaria no dia 23 o registro definitivo do imunizante, além do uso emergencial da vacina. No entanto, no dia da coletiva, o instituto adiou a apresentação dos resultados, após a farmacêutica chinesa pedir o envio dos dados para que sejam computados e apresentados de forma conjunta com testes realizados em outros países.
A vacinação será obrigatória?
Por 10 votos a 1, o Supremo Tribunal Federal (STF) definiu no último dia 17 que é obrigatória a vacinação contra a Covid-19, mas ninguém será vacinado a força. A União, os municípios, os 26 estados e o Distrito Federal estão liberados a criar leis para aplicar sanções a quem não quiser tomar a vacinar. Ou seja, a compulsoriedade será determinada por meio indireto. Quem recusar o imunizante poderá ser impedido de receber benefícios, frequentar espaços públicos ou assumir determinados cargos. O ministro Ricardo Lewandowski, relator do caso, votou a favor da vacinação compulsória e argumentou que ela já é obrigatória no Brasil. Todos os outros ministros do STF, com exceção de Kassio Nunes Marques, acompanharam integralmente o relator. O STF também determinou que os pais não estão desobrigados de vacinar os filhos por motivos ideológicos.
A obrigatoriedade das vacinação no Brasil já está prevista na lei 6.259, que instituiu o Programa Nacional de Imunizações (PNI). Essa compulsoriedade implica sanções como as previstas na Portaria nº 597, de 2004, que instituiu o calendário nacional de vacinação. Ali, é apontado que o indivíduo, não tendo completado o calendário, não poderá se matricular em creches e instituições de ensino, efetuar o alistamento militar ou receber benefícios sociais do governo. No entanto, não há outras medidas punitivas, como multa ou prisão, para quem optar por não se vacinar. A vice-presidente da Sociedade Brasileira de Imunizações (SBIm), Isabella Ballalai, ressaltou que essa obrigatoriedade já existe, mas argumentou que a discussão sobre a vacina da Covid-19 “é sem sentido”. “Não imagino ninguém armado ou prendendo alguém por não querer se vacinar. Mesmo a vacinação para outras doenças sendo obrigatória no país, nunca vi ninguém sendo interceptado para fazer isso”, afirmou. Já o professor de Imunologia do Curso de Farmácia e colaborador do Programa de Pós-graduação em Bioética da PUCPR, Sergio Surugi de Siqueira, diz ser contra a compulsoriedade. “Sou um entusiasta da vacina, tenho uma confiança quase que impossível de entender em relação à imunização. Porém, não cabe a ninguém obrigar a vacinação em adultos. Existe um principio na bioética que é a autonomia”, explicou.
Quem será vacinado primeiro?
No dia 16 de dezembro, o governo federal lançou o plano nacional de vacinação para a Covid-19. Por enquanto, a primeira etapa da imunização está dividida em fases e prevê vacinar 51 milhões de pessoas com 108,3 milhões de doses. O ministro da Saúde, Eduardo Pazuello, garantiu que todos os estados serão tratados da mesma forma. “Todos os brasileiros receberão a vacina de forma grátis, igualitária, proporcional. Não podemos brincar com a saúde da população brasileira”, disse. Os grupos prioritários serão divididos da seguinte forma:
- Fase 1
- Trabalhadores da saúde;
- Pessoas de 75 anos ou mais;
- Pessoas de 60 anos ou mais institucionalizadas;
- População indígena aldeado em terras demarcadas, povos e comunidades tradicionais ribeirinhas.
- Fase 2
- Pessoas de 60 a 74 anos.
- Fase 3
- Pessoas com morbidades — diabetes mellitus; hipertensão arterial grave; doença pulmonar obstrutiva crônica; doença renal; doenças cardiovasculares e cerebrovasculares; indivíduos transplantados de órgão sólido; anemia falciforme; câncer; obesidade grave (com IMC maior ou igual a 40).
Também constam como grupos prioritários povos quilombolas, trabalhadores da educação (professores e funcionários públicos e privados), pessoas com deficiência permanente severa, forças de segurança e salvamento, funcionários do sistema de privação de liberdade e a população privada da liberdade.
Toda a população poderá se vacinar em 2021?
Para os especialistas, não será possível vacinar toda a população brasileira em 2021. “A primeira ideia, além de proteger as pessoas, é descarregar o sistema de atendimento. Não acho que será possível vacinar todo mundo, mas poderemos voltar à normalidade em 2021″, disse o professor Sergio Surugi de Siqueira. No anúncio do plano de vacinação, o ministro Eduardo Pazuello informou que a imunização da população em geral deve ser concluída em 12 meses, mas que isso dependerá da quantidade de imunizante disponível — ou seja, o prazo pode ser de um total de 16 meses. Cada grupo prioritário deve finalizar a vacinação em aproximadamente 30 dias — totalizando quatro meses para os que foram definidos pelo ministério. Já quem não se enquadra em nenhum deles, vai precisar esperar. Segundo a vice-presidente da Sociedade Brasileira de Imunizações (SBIm), Isabella Ballalai, a emergência inicial é diminuir as hospitalizações e mortes por Covid-19. “Esse é o momento de salvar vidas, e o segundo momento é de eliminar e controlar o coronavírus”, afirmou. Algumas vacinas, como a de Oxford, a CoronaVac e a da Pfizer, precisam, ainda, de uma segunda dose, que deverá ser lembrada aos cidadãos brasileiros através do aplicativo ConecteSUS. Segundo o ministro Pazuello, a quinta e última fase do plano de vacinação consiste no monitoramento e rastreabilidade, visto que as vacinas possuirão previsões em sua bula de prazo distintos para a aplicação da segunda dose.
Depois da aprovação, mais algum ponto precisará ser definido?
Depois de uma vacina ter o seu registro ou uso emergencial aprovado pela Anvisa, a primeira etapa da vacinação deve iniciar em até cinco dias, segundo o governo federal. Ainda será necessário fazer o planejamento e coordenação das ações de logísticas de distribuição dos Estados e Distrito Federal para os municípios, que devem ser programadas pelas próprias unidades federativas, com o apoio do Ministério da Saúde. Nessa etapa, entram, por exemplo, a organização da compra de seringas, agulhas e preparação dos profissionais de saúde. Segundo o secretário de Vigilância em Saúde do Ministério da Saúde, Arnaldo Medeiros, o pregão está aberto para a compra de 330 milhões de seringas. “A expectativa é de que o fechamento do contrato seja 10 de janeiro, está tudo encaminhado”, garantiu. Paralelamente, ele disse que está sendo montado um curso para preparar os profissionais que vão atuar na vacinação. A vice-presidente da Sociedade Brasileira de Imunizações (SBIm), Isabella Ballalai, afirmou que espera que “nada atrase a vacinação”. “O PNI criou um grupo com dez eixos, cada um cuidando de um ponto que vai desde insumos, até quem será vacinado inicialmente. Eu acho que o bom é que o Brasil é um país com referências em campanha de vacinação, conseguimos chegar aos quatro cantos do país, o Brasil eliminou várias doenças assim. O PNI tem experiência, know how, então eu fico muito confortável quanto a isso”, disse.
As vacinas serão aprovadas para uso emergencial no Brasil?
China, Rússia, Reino Unido, Estados Unidos, Canadá, Suíça e Israel são alguns dos países que já começaram a vacinação para a Covid-19 em 2020. Os dois primeiros usam vacinas autorizadas apenas por seus próprios governos. A Rússia, com os imunizantes criados pelo Instituto Vector e pelo Instituto Gamaleya (Sputnik V), e a China, com as vacinas de três fabricantes: Sinopharm, CanSino e SinoVac (parceira do Instituto Butantan, em São Paulo). No entanto, nenhum desses imunizantes finalizou os estudos de fase 3. Já os demais países começaram a distribuir a vacina das farmacêuticas BioNTech e Pfizer, a maioria com registros para uso emergencial. O único país que liberou a vacina da Pfizer e da BioNTech por meio de um procedimento ordinário, e não por um aval de uso emergencial, foi a Suíça, no último dia 19. A Anvisa, segundo o professor de Imunologia do Curso de Farmácia e colaborador do Programa de Pós-graduação em Bioética da PUCPR, Sergio Surugi de Siqueira, é um órgão com protocolos rígidos para a aprovação de imunizantes no Brasil. “Tem que se fazer uma distinção entre registrar um produto, que é mais complexo, e aprovar em uso emergencial. A Anvisa aplica o rigor necessário e suficiente, para que as análises sejam feitas sem nenhum tipo de interferência”, explicou o especialista. A preocupação, para ele, é com os efeitos adversos. O Centro para Controle e Prevenção de Doenças (CDC, na sigla em inglês) informou, por exemplo, que seis pessoas desenvolveram uma reação alérgica grave chamada de anafilaxia após receberem a vacina contra a Covid-19 feita pela Pfizer e BioNTech. “Em uma situação dessas, se você não tiver nenhum outro viés, tem que se pesar sempre o risco e o benefício. Mesmo com medicações consagradas, aprovadas, com quantidades enormes de participantes, às vezes você descobre um problema em um medicamento cinco, 10 anos depois. Certeza absoluta sobre as vacinas não vamos ter. Porém, há elementos sólidos de que a vacina é segura e tem eficácia”, disse Siqueira. O “uso emergencial” é diferente do “registro sanitário”, já que o segundo depende de mais dados e da conclusão de todas as etapas de teste da vacina. No dia 14, a Anvisa informou que a análise de pedidos para o uso emergencial de vacinas será feita em um prazo de até dez dias. Além disso, tanto a Câmara dos Deputados quanto o STF determinaram que a Anvisa deve autorizar vacinas aprovadas por outras autoridades sanitárias internacionais, como as dos Estados Unidos (FDA) e da União Europeia (EMA).
Quantas doses o Brasil já adquiriu?
O Brasil deve receber 150 milhões de doses de vacinas contra a Covid-19 no primeiro semestre de 2021, somando os imunizantes Pfizer/BioNTech, Sinovac/Butantan e AstraZeneca/Fiocruz, afirmou no dia 22 de dezembro o secretário de Vigilância em Saúde do Ministério da Saúde, Arnaldo Medeiros. Deste total, de acordo com o ministro da Saúde, Eduardo Pazuello, 24,7 milhões seriam entregues já em janeiro. “Estamos falando, em janeiro, de 500 mil doses da Pfizer, nove milhões de doses do Butantan e 15 milhões a AstraZeneca. A data exata é o mês de janeiro. Pode ser 18, 20 de janeiro. Mas se nós pudermos compreender que o processo vai nos dar a data, já nos dá um novo desenho. Isso tudo dependendo do registro da Anvisa”, disse o ministro. O governo firmou memorandos de entendimento, que expõem a intenção de realizar acordos, com a Pfizer/BioNTech, Janssen, Instituto Butantan/Sinovac, Bharat Biotech, Moderna e Instituto Gamaleya. Com o Instituto Butantan e as farmacêuticas Bharat Biotech, Moderna, Gamaleya e Janssen, foram solicitadas informações de preços, estimativa e cronograma de disponibilização de doses, dados científicos dos estudos de fase I, II e III. Para a Pfizer/BioNTech, foi sinalizado interesse em 70 milhões de doses — sendo 2 milhões de doses previstas para o primeiro trimestre, 6,5 milhões no segundo trimestre; 32 milhões no terceiro trimestre e 29,5 milhões no quarto trimestre. Com a Janssen, a intenção é de 38 milhões de doses — 3 milhões de doses no segundo trimestre de 2021, 8 milhões no terceiro trimestre de 2021, 27 milhões no quarto trimestre de 2021. Já com a Pfizer, o total deve chegar a 70 milhões em 2021, 8 milhões no primeiro semestre e 62 milhões no segundo. Outro contrato também adiantado, segundo o Ministério da Saúde, é com o Instituto Butantan para 46 milhões de doses da CoronaVac – na manhã desta quinta-feira, 24, 5,5 milhões de doses do imunizante chegaram em São Paulo. A partir de janeiro, depois de aprovado por agência regulatória, serão adquiridas 9 milhões de doses em janeiro, 15 milhões em fevereiro e 22 milhões em março, de acordo com cronograma de entrega proposto pelo Butantan.



Comentários
Conteúdo para assinantes. Assine JP Premium.